近日,郑州大学河南先进技术研究院在肿瘤免疫治疗研究领域取得积极进展。研究团队创新性地开发出一种由红光/远红光调控的单个工程化细胞封装系统。该系统融合了合成生物学与生物材料技术,成功实现了活体水平下免疫因子表达的精准时空控制,具备可编程、可逆及低毒性等显著优势,为肺转移等难治性肿瘤的治疗提供了新的解决方案。
恶性肿瘤肺转移是导致全球癌症相关死亡的主要原因之一。尽管工程化免疫细胞疗法在转移性肿瘤治疗中展现出巨大潜力,但其实际应用仍受制于细胞因子风暴、脱靶效应以及宿主免疫清除等严峻挑战。因此,如何在显著延长细胞在肿瘤部位驻留时间的同时,实现对治疗过程的实时可逆调控,成为该领域亟待突破的关键科学难题。
针对上述问题,研究团队成功构建了一套具备“感知—响应”功能的智能细胞控制系统。该系统利用植物来源的光敏蛋白ΔPhyA-PCB作为核心元件:在红光(660 nm)激发下,ΔPhyA能与FHY1蛋白发生异源二聚化,进而启动下游效应分子(包括IFN-γ、CD47抗体及IL-6)的高效表达;反之,在远红光(730 nm)照射下,二聚体迅速解离,蛋白表达即时阻断。这种光控“分子开关”表现出优异的可逆性与稳定性,历经多轮光照循环仍能保持高效响应,从而实现了对免疫治疗剂释放过程的精准时空“可控性”。
体内药效评估显示,在4T1-luc小鼠肺转移模型中,经红光/远红光精准调控的单细胞封装治疗组展现出卓越的抗肿瘤转移效力。相较于持续表达细胞因子的传统策略或未封装的工程化细胞,该智能系统在维持高效抗瘤活性的同时,未诱发明显的全身系统性毒性或血液学异常,实现了治疗“有效性”与“安全性”的完美解耦。该研究建立了一种闭环可控的活细胞治疗范式,将工程细胞转化为可在体内远程调控的 “活体药物工厂”。
相关研究成果以“On-demand cancer immunotherapy via single-cell encapsulation of synthetic circuit-engineered cells”为题,发表在国际知名期刊《Science Advances》上,论文第一作者为河南先进技术研究院硕士研究生赵月和郑州大学第一附属医院李锐。通讯作者为我院陈亚州副研究员和国家纳米中心聂广军研究员,郑州大学河南先进技术研究院为第一单位。该研究获得了国家自然科学基金、博士后国际交流项目等的支持。
文章链接:https://www.science.org/doi/10.1126/sciadv.aea3573
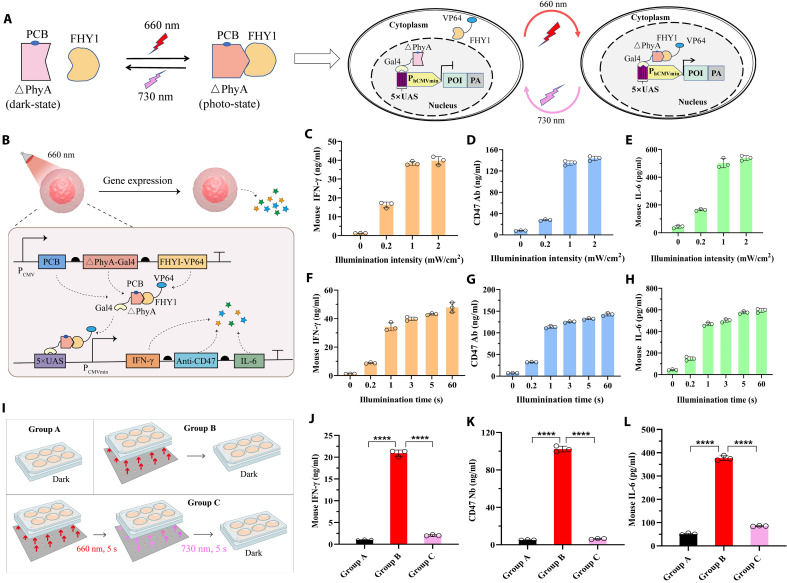
郑州大学河南先进技术研究院在细胞肿瘤免疫治疗研究领域取得积极进展