近日,郑州大学生命科学学院于政权团队在睡眠障碍影响肠干细胞的神经内分泌途径研究方面取得积极进展。该研究首次系统阐明了睡眠障碍通过神经内分泌途径直接调控肠干细胞的机制,为理解“脑—肠轴”在慢性疾病中的作用提供了关键证据,也为开发睡眠相关肠道疾病的干预策略提供了新思路。
研究发现,位于延髓的DMV是大脑中对睡眠剥夺高度敏感的关键神经核团。睡眠不足可异常激活DMV神经元,增强迷走神经向肠道释放乙酰胆碱;乙酰胆碱进一步作用于肠上皮细胞的毒蕈碱型受体,促使肠嗜铬细胞大量释放五羟色胺(5-HT),并抑制其再摄取,导致肠道局部5-HT急剧升高;过量的5-HT激活肠道干细胞表面的HTR4受体,引发显著的氧化应激和整合应激反应,从而损害了肠道干细胞的自我更新和再生能力。动物实验显示,睡眠剥夺仅两天即可使小鼠肠道干细胞数量减少一半。
虽然5-HT长期以来被视为中枢神经递质,但事实上约95%的体内5-HT来源于肠道。作为重要的外周信号分子,5-HT广泛参与胃肠运动、代谢调节、免疫稳态及血管功能维持。因此,睡眠障碍诱发的外周5-HT急剧升高,可能不仅损害肠道屏障,还会通过循环系统对肝脏、胰腺及心血管系统产生连锁影响,成为多器官功能紊乱的潜在驱动因素。在干预层面,研究团队发现多种靶向该通路的策略具有保护作用,包括阻断毒蕈碱受体信号的阿托品、抑制HTR4的特异性拮抗剂GR113808,以及抗氧化剂维生素C,均能在不同程度上缓解睡眠障碍引发的肠道损伤。
相关研究成果以“Sleep disturbance triggers aberrant activation of vagus circuitry and induces intestinal stem cell dysfunction”为题发表在国际知名期刊《Cell Stem Cell》上。郑州大学生命科学学院于政权教授、中国科学院深圳先进技术研究院脑认知与脑疾病研究所王枫研究员、中国农业大学营养与健康研究院吕聪教授和美国加利福尼亚大学欧文分校发展与细胞生物学系教授Maksim V. Plikus为该论文的共同通讯作者。该团队张明鑫博士、吴茜博士、博士生刘笛为该论文共同第一作者。
原文链接:
https://doi.org/10.1016/j.stem.2026.01.002
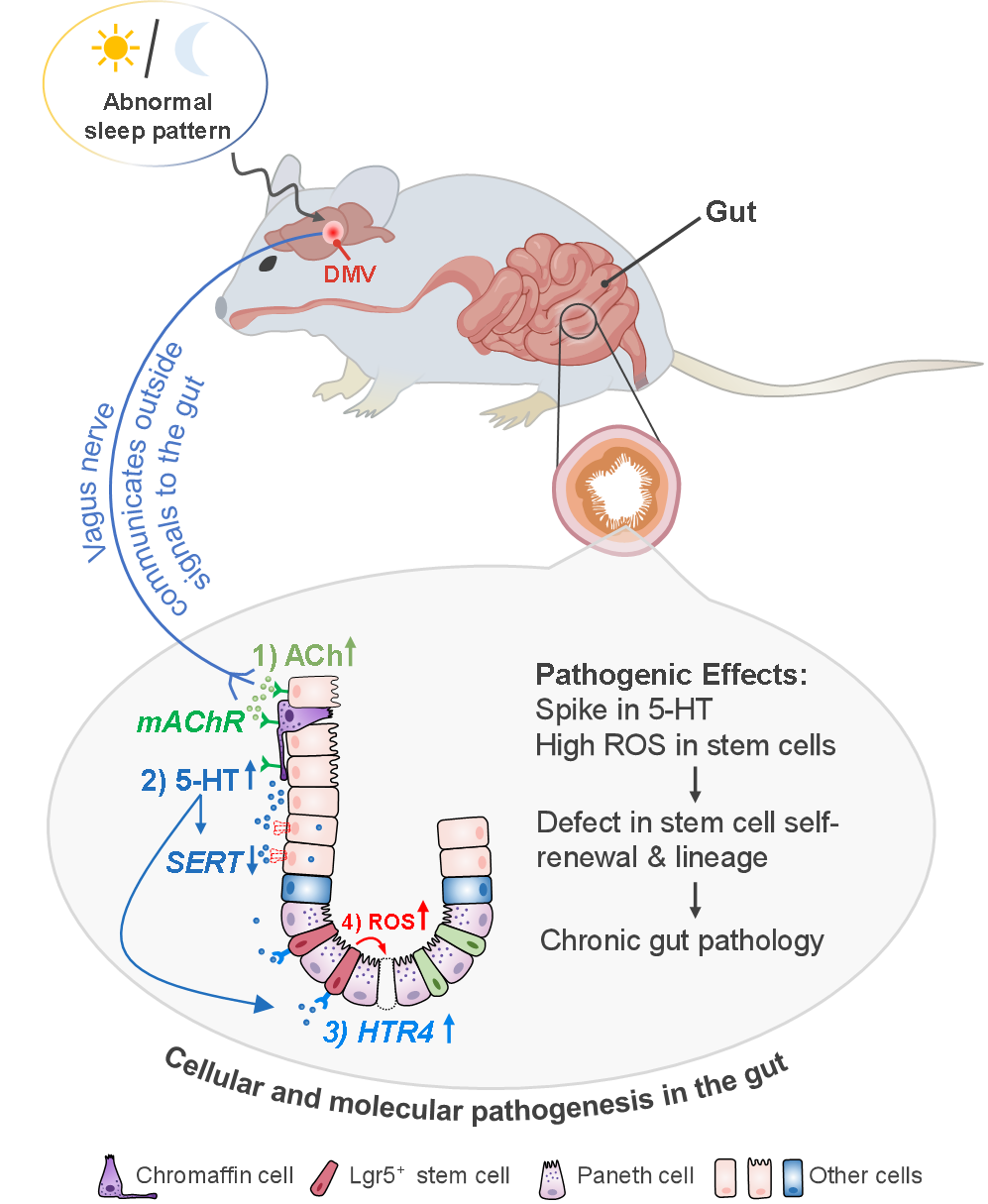
郑州大学生命科学学院在睡眠障碍影响肠干细胞的神经内分泌途径研究方面取得积极进展