近日,郑州大学董子钢教授团队在肿瘤精准治疗领域接连取得重大原创性突破,两项研究成果分别发表于《Nature Communications》与《PNAS》两大国际顶级学术期刊。该研究系统揭示了食管鳞癌、胃癌化疗抵抗的关键分子机制,成功发现全新疗效预测生物标志物与治疗靶点,为推动肿瘤个体化精准治疗、提升患者化疗获益提供了重要理论与实践依据。
新辅助化疗已广泛应用于食管癌、肺癌和乳腺癌等多种肿瘤的治疗,可显著提高患者5年生存率。然而,约50%–70%的患者对新辅助化疗不响应,不仅限制了治疗获益,还需承受化疗相关毒副作用,严重影响预后。因此,阐明影响新辅助化疗疗效的关键分子机制,开发预测化疗疗效的生物标志物以及联合治疗靶点,对于提升治疗效果具有重要意义。
在食管鳞癌化疗抵抗研究中,发现INCENP和CDCA8在新辅助化疗不敏感的食管鳞癌、肺癌及乳腺癌患者活检组织中高表达,且与不良生存预后密切相关,可有效预测新辅助化疗反应性。分子机制层面,METTL3介导INCENP和CDCA8的m6A修饰,被YTHDF3识别后并促进其翻译,从而增强肿瘤细胞对紫杉醇和顺铂的耐受性。此外,抑制INCENP和CDCA8可显著提高肿瘤对化疗的敏感性,显示出良好的治疗靶点潜力。该研究系统阐明了肿瘤新辅助化疗抵抗的关键分子机制,为预测新辅助化疗反应性提供了可靠的生物标志物及联合治疗靶点,对推动肿瘤个体化精准治疗具有重要意义。该研究成果以《INCENP and CDCA8 predict neoadjuvant chemotherapy response and outcomes in esophageal squamous cell carcinoma》为题发表于顶尖期刊《Nature communications》。郑州大学、中美(河南)荷美尔肿瘤研究院董子钢教授和郑州大学附属肿瘤医院赵四敏副教授为该文章的共同通讯作者,博士研究生王翔宇和王婷为论文的共同第一作者,由郑州大学、中美(河南)荷美尔肿瘤研究院、天健先进生物医学实验室共同完成。
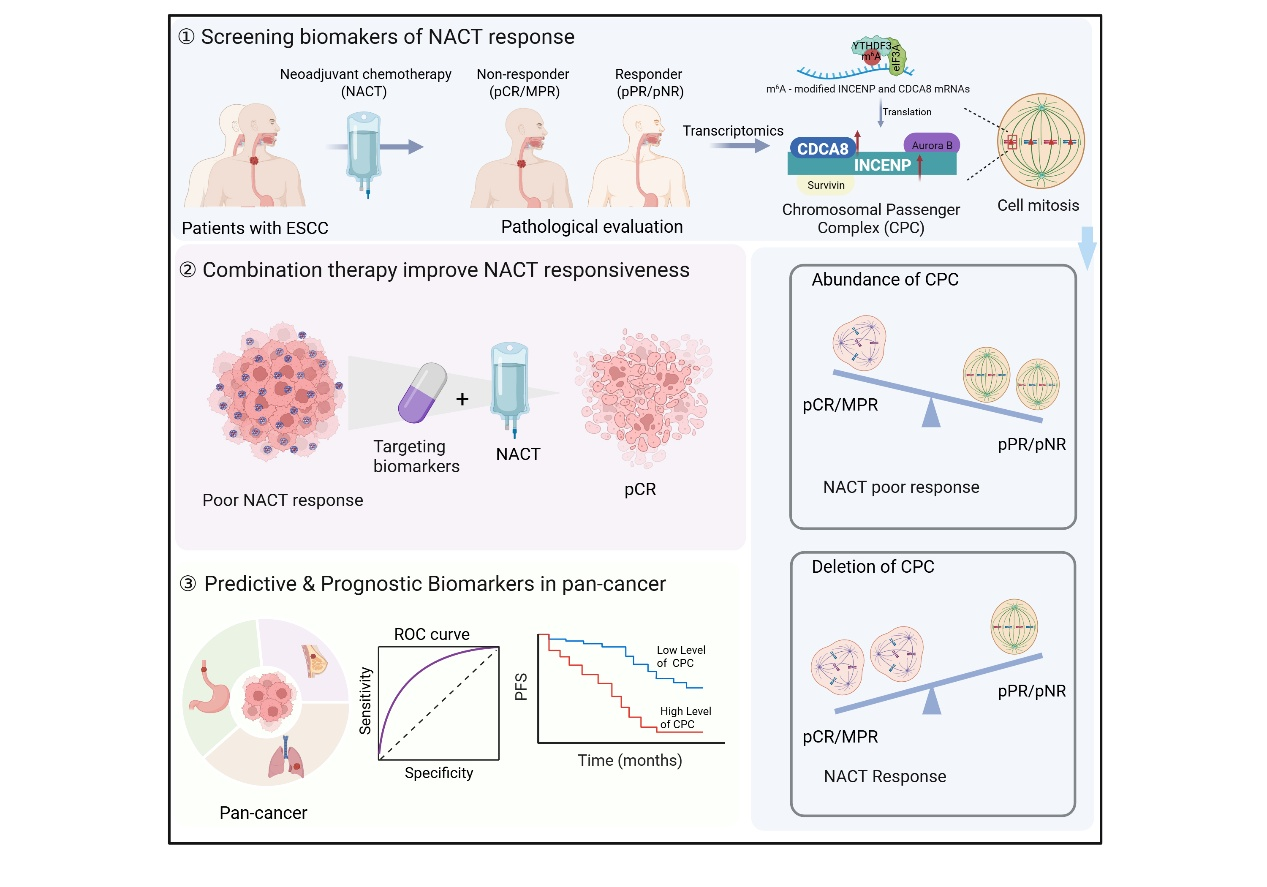
图1:INCENP和CDCA8预测食管鳞癌新辅助化疗反应性的机制示意图
文章链接:
https://www.nature.com/articles/s41467-026-68371-x
在胃癌代谢与化疗耐药研究中,发现胃癌组织中丝氨酸代谢显著异常,关键限速酶PHGDH的表达和活性明显升高,并受到上游激酶WNK1的直接调控。WNK1通过在PHGDH的Ser349和Ser371位点发生磷酸化修饰,增强其酶活性和蛋白稳定性,进而驱动丝氨酸代谢重编程,提升肿瘤细胞抗氧化防御和DNA损伤修复能力,降低其对奥沙利铂的治疗敏感性。进一步结合患者队列、类器官和动物模型研究表明,PHGDH磷酸化水平及丝氨酸代谢活性与奥沙利铂治疗反应密切相关,有望成为评估胃癌代谢脆弱性和化疗响应的潜在“双重生物标志物”。该研究揭示了“WNK1–PHGDH–丝氨酸代谢轴”在胃癌进展和化疗耐药中的重要作用,也为临床识别优势获益人群、优化新辅助化疗策略和开发联合干预方案提供了重要依据。该研究成果以《PHGDH phosphorylation mediated by WNK1 serves as a dual marker of metabolic vulnerability and responsiveness to oxaliplatin treatment》为题发表于顶尖期刊《PNAS》。郑州大学、中美(河南)荷美尔肿瘤研究院董子钢教授,阜外华中心血管病医院郭智萍教授、晋果果副教授担任共同通讯作者,博士研究生方少伯为论文的第一作者,由郑州大学、中美(河南)荷美尔肿瘤研究院、天健先进生物医学实验室共同完成。
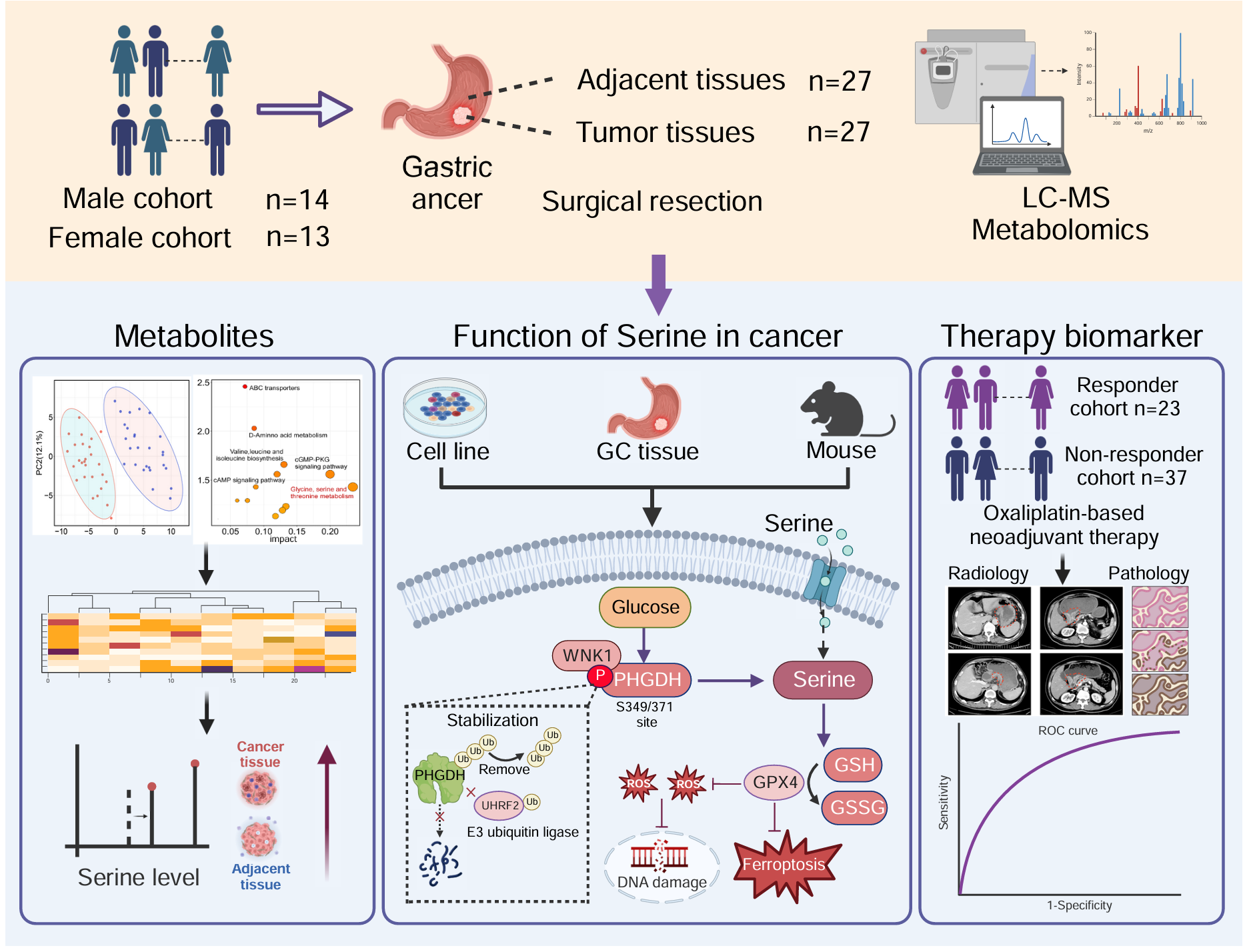
图2:WNK1介导的PHGDH磷酸化作为代谢脆弱性和对奥沙利铂治疗反应性双重标志物的机制示意图
文章链接:
https://www.pnas.org/doi/10.1073/pnas.2525213123